1. Arterien des Gehirns
Die Gefäßversorgung des Gehirns erfolgt durch die beiden inneren Halsschlagadern (A. carotis interna) und die beiden Wirbelschlagadern (A. vertebralis), die sich nach Eintritt in die Schädelhöhle zur A. basilaris vereinigen (Vertebralis-Basilariskreislauf). Diese Gefäße bilden ein großes Anastomosensystem (im Subarachnoidalraum) an der Hirnbasis, den Circulus arteriosus cerebri (Willisi).
1.1 Karotiskreislauf
Die A. carotis interna (ACI) geht an der Gabelung der A. carotis communis ab, zieht neben der Pharynxwand nach oben und tritt im Canalis caroticus durch die Schädelbasis. Während des Verlaufs zwischen Hals und Schädelbasis gibt die ACI (im Gegensatz zur A. carotis externa, ACE) keine Äste ab. Nach einer S-förmigen Krümmung (Karotissyphon) taucht sie an der Medialseite des Prc. clinoideus anterior auf und durchbohrt die Dura mater. Im Subarachnoidalraum teilt sie sich in die Hauptäste: A. cerebri ant. und A. cerebri med.
1. Die A. cerebri ant. (ACA) verläuft nach vorn und medial und zieht im Hemisphärenspalt zwischen beiden Frontallappen über dem Balken nach hinten. Über die A. communicans ant. steht sie mit dem entsprechenden Gefäß der Gegenseite in Verbindung. Ihre Kortexäste versorgen die Medialseite bis zum Sulcus parieto-occipitalis und einen fingerbreiten Streifen der angrenzenden Konvexität. Damit versorgt dieses Gefäß die Fußregion des G. praecentralis.
Die A. cerebri med. (ACM) verläuft zunächst auf der Hirnbasis lateralwärts. Hier gibt sie einige wichtige zentrale Äste ab. Sie zieht dann im Sulcus lateralis der Seitenfläche der Hemisphären. Die Kortexäste versorgen die gesamte Seitenfläche mit Ausnahme des genannten Versorgungsgebietes der A. cerebri anterior, sowie des Okzipitalpols und der Unterseitenfläche, die von der A. cerebri posterior versorgt werden. Die gesamte motorische Region (mit Ausnahme der Fußregion) wird damit von der ACM versorgt. Die zentralen Äste ziehen in die Basalganglien des Vorderhirns.
Neben diesen Hauptästen gehen zwei weitere Gefäße aus der ACI hervor: Die A. ophthalmica geht dort ab, wo die ACI den Sinus cavernosus verläßt. Ihr wichtigster Ast ist die A. centralis retinae, die an der Papilla n. optici in den Augapfel eintritt und die dem Glaskörper zugewandten Netzhautschichten versorgt. Die A. choroidea ant. geht kurz vor der Aufzweigung der ACI in die Zerebralarterien ab. Sie versorgt neben dem Plexus choroideus die Capsula interna und Teile der Sehbahn.
1.2 Vertebralis-Basilariskreislauf
Die A. vertebralis entspringt aus der A. subclavia; sie steigt im Hals durch die Öffnungen der Querfortsätze der (6.-1.) Halswirbel zum Trigonum vertebrale auf und tritt durch das Foramen magnum in die Schädelhöhle. Auf dem Clivus vereinigt sie sich mit dem korrespondierenden Gefäß der Gegenseite zur A. basilaris. Durch Teilung der A. basilaris entsteht die A. cerebri posterior (ACP) am Vorderrand der Brücke, vor dem Austritt des CN III. Vorher gehen aus der A. vertebralis und A. basilaris 3 Äste zur Versorgung des Kleinhirns ab. Die ACP verläuft parallel zum Tentoriumrand um die Hirnschenkel.
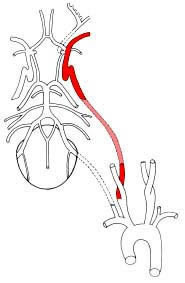
Abb. 22-3: Schematische Darstellung des Karotis- und des Vertebro-Basilaren Kreislaufs mit ihrem Anastomosensystem an der Hirnbasis




Legende
Die A. vertebralis durchbricht die M. atlanto-occipitalis und die Dura mater, verläuft durch das For. occipitale mg. in die hintere Schädelgrube und vereint sich auf dem Clivus mit dem Gefäß der Gegenseite zur A. basilaris. Auf der Höhe des Vorderrandes der Pons spaltet sich dieses Gefäß in die paarige A. cerebri posterior (ACP) auf. Die ACP versorgt den gesamten Hinterhauptslappen einschließlich des Sehzentrums. Aus embryologischen Gründen ist das Vertebro-Basilar-System variabel.
1.3 Circulus arteriosus cerebri (Willisi)
Zwischen dem rechten und linken Karotiskreislauf und dem Vertebro-Basilariskreislauf gibt es ein wichtiges Anastomosensystem: über die A. communicans posterior sind beide Stromgebiete miteinander verbunden; über die A. communicans anterior wird der Gefäßring zwischen beiden Zuflüssen der ACI geschlossen. Dieser Gefäßring, der den Hypothalamus umgibt, erlaubt, daß Blut aus jedem Zuflußgebiet in jedes Areal des Gehirns verteilt wird. Von ihm geht die Versorgung der kortikalen (Rr. corticales) und subkortikalen Areale (Rr. basales) ab. Ganz im Gegensatz zu der großen Flexibilität, die hier besteht, stellen die Äste, die aus dem C. arteriosus Willisi entspringen, Endarterien dar, und es finden sich zwischen ihnen (fast) keine Anastomosen. Bei einem Gefäßverschluß ist die Ernährung des versorgten Bezirks daher nicht gesichert. Dagegen sind die dem Circulus arteriosus Willisi benachbarten Areale des Hypothalamus und der Hypophyse gut gegen vaskuläre (Versorgungs-) Krisen geschützt.
Abb. 22-4: Darstellung des Gefäßverlaufs des intrakraniellen Abschnitts des Vertebro-Basilaren Systems und seiner Versorgungsgebiete.

Legende
Die drei longitudinalen Versorgungszonen sind durch Markierungen getrennt.
Legende
Die ACA verzweigt sich auf der medialen Seite der Großhirnhemisphären und greift auf ein etwa fingerbreites Areal über die mantelkante auf die Lateralfläche über. Die ACM versorgt die zentrale Fläche der seitlichen Hemisphärenwand. Hierzu gehört die Versorgung von Sprachzentrum, Zentrum für den Arm und mimische Gesichtsmuskulatur, sowie das Hörzentrum.
2. Arterien des Rückenmarks
Zur Versorgung des Rückenmarks gibt es sowohl longitudinal wie transversal (segmental) verlaufende Gefäße. Die längs verlaufenden Gefäße entstammen aus der A. vertebralis und werden durch die unpaare A. spinalis anterior und die beiden paarigen Aa. spinales posteriores gebildet. Die A. spinalis anterior verläuft median im Sulcus medialis ant., die Aa. spinales post. an der Eintrittsstelle der hinteren Wurzel.
Die segmentale Versorgung erfolgt aus (interkostalen u.a.) Ästen von Arterien, die außerhalb der Wirbelsäule liegen. Sie treten als kleine segmental verlaufende Arterien durch die Foramina intervertebralia in den Wirbelkanal ein. Jede segmentale A. spinalis teilt sich in eine A. radicularis ant. und post., die jeweils mit den Nervenwurzeln verlaufen und mit den längs verlaufenden Gefäßen anastomosieren. Verlauf und Volumen der Rückenmarksarterien sind sehr variabel.
Legende
Abk.:
1, Aorta,
2, Aortenbogen,
3, A. subclavia,
4, A. vertebralis,
5, A. basilaris,
6, A. spinalis ant., R. descendens,
7, A. spinalis ant., R. ascendens,
8, A. radicularia magna,
3. Blut-Hirnschranke
Das ZNS wird in vieler Hinsicht vom restlichen Körper abgegrenzt und lebt in einem Zustand herausragender Isolierung. Diese Kontrolle ist hauptsächlich durch ein Barrierensystem zwischen dem Gefäßsystem und dem Nervensystem (Blut-Hirn-/Nervenschranke), sowie dem Liquorraum (Blut-Liquorschranke) gebildet.
Der Ort der Blut-Hirnschranke wird durch die Hirnkapillaren gebildet. Sie sind besonders gebaut, so daß sie den Substanz- und Stoffaustausches zwischen Blut und Gehirn begrenzen. In den Hirnkapillaren gibt es zwei Besonderheiten: Ihre Endothelzellen bilden ein kontinuierliches, nicht fenestriertes Endothel, das den transkapillären Transport von Substanzen zwischen Blut und Gehirn stark einschränkt. Hierdurch erfolgt eine strenge Selektion der in das Hirnparenchym eintretenden Substanzen. Ferner besteht eine innige Beziehung zwischen der luminalen Seite der Mikrogefäße (Endothelzellen) und der abluminalen Seite (Astrozyten des Gehirns). Mit wenigen Ausnahmen sind die Mikrogefäße praktisch komplett durch Astrozytenprozesse umgeben. Der enge Kontakt der Astrozyten sowohl mit Endothelzellen als auch mit Neuronen legt eine Mittlerrolle für den Substanztransport nahe. Eine Verletzung der Kapillaren führt zu einem Austreten von Plasmaproteinen und provoziert ein vasogenes Hirnödem.
4. Venen
4.1. Venen des Gehirns
Die Venen des Gehirns besitzen einen dünnen Wandaufbau und keine Klappen. Sie treten aus dem Gehirn und liegen in den weichen Hirnhäuten. Die Hirnvenen bilden ein oberflächliches und ein tiefes Venensystem, das sich jeweils völlig unabhängig von den Arterienstämmen verhält. Das oberflächliche System wird durch die Venen der Hirnoberfläche gespeist. Sie drainieren entweder nach oben in den S. sagittalis superior oder nach unten in die Sinus der Schädelbasis. Als sogenannte Brückenvenen ziehen sie durch den Subarachnoidalraum zu den Sinus durae matris. Das tiefe System setzt sich aus dem Zuflußgebiet des S. rectus zusammen. In ihn münden die V. cerebri magna und die Venen der Ventrikelwand.
Sinus durae matris:
Bevorzugt an den Stellen, wo die Duraduplikaturen septenartig in die Schädelhöhle hineinragen, kommt es zur Bildung von Blutleitern, die als Sinus durae matris (kurz: Sinus) bezeichnet werden. Aufgrund dieser Anordnung sind sie auf einem Querschnitt annähernd triangulär. In sie entleeren sich die oberflächlichen zerebralen Venen (siehe Kap. 23).
Die wichtigsten Sinus finden sich entlang der Anhaftung von Falx cerebri und Tentorium cerebelli. Es sind der Sinus sagittalis superior, der rechte und linke Sinus transversus und an der Oberkante des Tentoriums der Sinus rectus. Alle 4 Sinus münden in den Confluens sinuum (auch Torcular bezeichnet), der an der Protuberantia occipitalis interna gelegen ist. Vom Confluens sinuum fließt das venöse Blut durch den Sinus transversus und Sinus sigmoideus in die V. jugularis interna. (Die weiteren Sinus besitzen keine klinische Bedeutung).
Einen Sinus anderer Bauart, der eher einem venösen Gefäßkomplex gleicht, bildet der Sinus cavernosus. Er ist anatomisch, funktionell und klinisch sehr wichtig. Er liegt zu beiden Seiten des Corpus ossis sphenoidalis, ist aber quer mit der gegenseitigen Struktur verbunden, so daß er die Hypophyse zirkulär umgibt. Von vorne nimmt dieser Sinus die V. ophthalmica inf. und die zentrale Netzhautvene auf. Nach hinten hat er Verbindung mit dem Sinus transversus. Außerdem ist er mit dem Plexus pterygoideus an der äußeren Schädelbasis verbunden. In ihn münden die Gefäße der Hypophyse.
Legende
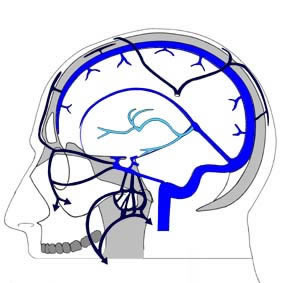
Venöses Blut aus dem Cortex cerebri und der äußeren Hälfte des Album wird in das oberflächliche Venensystem abgeleitet. Venöses Blut aus dem tiefen Album und den tiefen Grisea gelangt über das tiefe Venensystem (V. magna Galeni, S. sagittalis inf., S. rectus) in den Confluens sinuum.
4.2 Venen des Rückenmarks
Der venöse Abfluß erfolgt zunächst in 6 längs-verlaufende, stark gewundene Kanäle, in ihrer Gesamtheit den Plexus vertebralis bilden und mit dem venösen System der Hirnvenen und Sinus des Schädels anastomosieren.
5. Angewandte Anatomie
5.1 Intrakranielle Blutungen
Tabelle 22-1: Schematische Darstellung der Hirnhäute und der meningealen Blutungen (Fanconi Abb. p. 910)
| Epidurale Blutung | Subdurale Blutung | Subarachnoidale Blutung | |
| Definition | Arterielle Blutung zwischen der Tabula interna des Schädeldaches und der Dura mater (meist A. meningea media) | Venöse Blutung zwischen Dura mater und Arachnoidea | Arterielle Blutung zwischen Arachnoidea und Pia mater (Subarachnoidalraum) |
| Ursache | schweres Schädeltrauma | Schädeltrauma (evtl. Bagatelltrauma) oft in Kombination mit Gefäßbrüchigkeit | Blutung aus einem rupturierten Hirngefäßaneurysma |
| Symptome neben Hirndruckerscheinungen | häufig längeres beschwerdearmes Intervall | blutiger Liquor |
5.2 Durchblutungsstörungen und Blutungen im Gehirn und Rückenmark
Bei den akuten Durchblutungsstörungen sind solche im Großhirnbereich (Schlaganfall, Apoplex), im Vertebro-Basilar-Bereich, im Hirnstamm und Rückenmark zu unterscheiden.
Der Schlaganfall ist die dritthäufigste Todesursache in der Bundesrepublik und die häufigste Ursache der Invalidität überhaupt. Er kann durch einen Verschluß einer Hirnarterie (anämischer Infarkt), durch eine Massenblutung oder durch eine Hirnvenenthrombose ausgelöst werden. Die Symptomatik des Schlaganfalls wird wesentlich von der Topographie der Durchblutungsstörung bestimmt. Bei einer Unterbrechung der kortikalen Projektionsfasern in der inneren Kapsel kommt es zunächst zu einer schlaffen Lähmung der betroffenen Gebiete auf der Gegenseite, die später in eine spastische Lähmung übergeht.